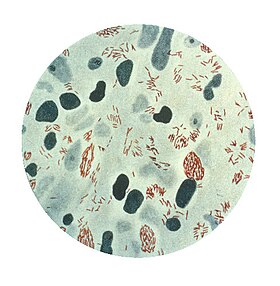
Mycobacterium leprae
| Mycobacterium leprae | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Classificação científica | |||||||||||||||
| |||||||||||||||
| Nome binomial | |||||||||||||||
| Mycobacterium leprae Hansen, 1874 | |||||||||||||||
Mycobacterium leprae ou bacilo de Hansen é uma actinobactéria, responsável pela hanseníase (lepra), pertencendo ao gênero Mycobacterium. Possui crescimento extremamente lento quando comparado com outras bactérias.
Bacilos de tamanho médio variando entre 0,3 e 0,5 μm de diâmetro e 4,0 a 7,0 μm de comprimento. A temperatura ótima de crescimento é em torno de 30ºC, motivo pelo qual a bactéria infecta regiões mais frias do corpo (extremidades). Seu cultivo não pode ser realizado em meio de cultura como outras micobactérias, podendo ser inoculada em camundongos ou tatus selvagens.
Possui a habilidade de sobreviver e crescer dentro de macrófagos, e seus fatores de virulência protegem o bacilo de formas tóxicas de oxigênio, sendo obrigatoriamente patógena. [1]
A micobactéria parasita os macrófagos e as células de Schwann que formam a mielina dos nervos periféricos. A destruição da mielina leva à disfunção dos nervos, isto faz com que a pessoa perca o tato.
O sistema imunitário reage eficazmente às micobactérias pela formação de granulomas. O tipo de reação imunitária ao M. leprae é extremamente importante na progressão da lepra. Esta bactéria sobrevive à fagocitose e multiplica-se inclusivamente dentro dos macrófagos. Se houver uma reacção TH1, citotóxica, com formação de granulomas sequestradores da bactéria e com destruição dos macrófagos infectados, a doença torna-se quase benigna e não é capaz de progredir: é a lepra tuberculóide. Se no entanto for ativada uma resposta TH2, com produção de anticorpos, não há formação de granulomas e a bactéria dissemina-se, surgindo a lepra típica, ou lepra lepromatosa. Quando isso ocorre, as bactérias passam a atuar no sistema nervoso central.
Epidemiologia e Transmissão
[editar | editar código-fonte]A M. leprae é transmitida pelo contato direto com doente não tratado, através das vias aéreas. Sua incubação é lenta, de 2 à 7 anos, e sua patogenicidade é considerada baixa.
Os fatores epidemiológicos não são certos, uma vez que o contato com o bacilo não necessariamente leva à infecção ou à doença, que ocorre em apenas 10% dos casos. Diferentes organismos apresentam diferentes respostas imunológicas que levam à infecção ou não, essa resposta é afetada por contato prévio com M. tuberculosis e pela imunização pela BCG.
A transmissão de M. leprae está ligada à diversos fatores socioeconômicos, como a falta de acessibilidade ao diagnóstico e tratamento, uma vez que este impede a transmissão do bacilo; alta densidade populacional, que promove contato direto com doentes; e condições precárias de higiene. [2][3]
Diagnóstico
[editar | editar código-fonte]O diagnóstico da Hanseníase (Lepra) é feito observando os sintomas físicos, que são muito característicos, raramente sendo preciso realizar outros exames. São feitas analises das lesões cutâneas, palpações dos nervos, avaliações da sensibilidade superficial e da força muscular dos membros superiores e inferiores. [4]
Em casos de dúvida, pode ser feito uma biópsia da área ou exames laboratoriais para medir a quantidade de bacilos presentes na amostra.
Inoculação
[editar | editar código-fonte]A Mycobacterium leprae foi descoberta por Gerhard Armauer Hansen e foi a primeira bactéria a ser relacionada a uma doença humana. Embora tenha sido descoberta em 1873, até hoje não é possível cultivá-la em laboratório e esse fator é considerado como um dos principais empecilhos para a erradicação da hanseníase.
O melhor método já desenvolvido para tentar demonstrar a multiplicação da M. leprae em laboratório é a técnica de Shepard, desenvolvida em 1960: para realização desta técnica bacilos de pacientes com hanseníase não-tratados são inoculados na pata de camundongos imunocompetentes. A partir dos resultados observados, chegou-se ao consenso de que a melhor temperatura para o crescimento do bacilo possa ser entre 27°C e 30°C, suportando a hipótese de que os bacilos tenham predileção por temperaturas abaixo da média corporal humana de 37°C uma vez que as lesões dos pacientes acometidos pela hanseníase geralmente são localizadas na pele, mucosa nasal e nervos periféricos.[5]
Biossegurança
[editar | editar código-fonte]A M.leprae faz parte da Classe de risco 2. Essa classificação leva em conta o risco potencial oferecido pelo patógeno ao indivíduo, à comunidade e ao meio ambiente, e permite que se faça a classificação do Nível de Biossegurança (NB) do patógeno levando em conta também o tipo de manipulação a ser realizada pelo laboratório. A M.leprae corresponde ao NB 2.
Além disso, o fato de essa bactéria não poder ser cultivada em meios de cultura torna necessária a utilização de animais. Isso implica que esses laboratórios tenham que se enquadrar também no Nível de Biossegurança com Animais 2.
Nesses laboratórios, além de controle rigoroso de descarte, existe a utilização de barreiras físicas primárias (cabine de segurança biológica e equipamentos de proteção individual) e secundárias (desenho e organização do laboratório). [6]
Genoma
[editar | editar código-fonte][7]Apenas 49,5% dos genes da M. leprae são ativos, sendo que o restante se divide em pseudogenes (genes teoricamente normais, mas não funcionais – 27%) e genes não codificantes (23,5%). Quando comparado ao genoma da M. tuberculosis, que apresenta aproximadamente 90% de genes funcionais, percebe-se que a M. leprae sofreu uma redução gênica, fruto de um processo de evolução redutiva. Por ter muitos genes em comum com a M. tuberculosis (por volta de 1400), presume-se que o genoma da M. leprae já foi muito semelhante ao das outras micobactérias.
Esse tipo de processo evolutivo é comum em parasitas celulares obrigatórios: os genes são desativados, pois suas funções não são mais necessárias à sobrevivência de tais seres. Isso pode ter feito com que a M. leprae perdesse diversas vias metabólicas essenciais a sua sobrevivência fora do hospedeiro, explicando então porque ainda não foi possível cultivar a bactéria in vitro.
Fatores de virulência
[editar | editar código-fonte]A M. leprae tem a habilidade de invadir o sistema nervoso periférico (SNP) causando diversas neuropatias, sendo seu principal alvo as células de Schwann (células que constroem mielina dos axônios).
Embora não sejam muito claros os mecanismos pelos quais a M. leprae se aloja nas células de Schwann, estudos indicam que a bactéria é ingerida assim que se adere à tais células, no entanto estas não são capazes de digerir o parasita. Então dentro da célula a M. leprae pode alterar a expressão de genes das células de Schwann, alterando a produção de mielina. Além de servir como hospedeira para o parasita as células de Schwann também o protege das respostas imunes encadeadas pela sua presença.
Sendo que a bainha de mielina é responsável pelo chamado impulso saltatório, quando os nervos são lesados há o retardamento da transmissão dos impulsos nervosos, especialmente os de sensibilidade. Isso caracteriza uma das principais características da hanseníase. [8]
Produção de células indiferenciadas
[editar | editar código-fonte]Para analisar melhor como a bactéria afeta as células de Schwann, foram feitos estudos com células de Schwann de ratos adultos infectadas com M. leprae e isoladas in vitro. Foi observada a mudança na regulação de diversos genes em resposta à infecção: houve maior expressão dos genes relacionados ao desenvolvimento embrionário e menor expressão daqueles relacionados à diferenciação celular. Mais especificamente, a célula se mostrou capaz de exportar para fora do núcleo o principal fator de transcrição regulador da diferenciação das células Schwann, o SOX10, indicando que a infecção pela bactéria desequilibra eventos de transcrição específicos das células de Schwann.
Isso mostra que a M. leprae desencadeia a plasticidade das células de Schwann, ou seja, reverte-as ao seu estado imaturo. Como as células indiferenciadas são capazes de migrar para diferentes áreas do corpo, a bactéria vai junto com elas. Isso possibilita a infecção de diferentes tecidos, como o músculo esquelético por exemplo.
Os mecanismos que desencadeiam esta reprogramação celular ainda não foram elucidados, mas acredita-se que isso possa acontecer em outras doenças infecciosas. Novas descobertas nessa área podem melhorar não só o tratamento da hanseníase, permitindo o diagnóstico nos estados iniciais da doença, mas também possibilitar o uso da M. leprae para transformar células diferenciadas em células-tronco, e isso poderia revolucionar o tratamento de doenças degenerativas como Alzheimer. [9][10]
Ver também
[editar | editar código-fonte]- Mycobacterium lepromatosis, descoberto em 2008
Referências
[editar | editar código-fonte]- ↑ Trabulsi, Luiz Richard (2008). Microbiologia. [S.l.]: Atheneu
- ↑ «Mycobacterium leprae–millennium resistant! Leprosy control on the threshold of a new era»
- ↑ «Spatial and temporal epidemiology of Mycobacterium leprae infection among leprosy patients and household contacts of an endemic region in Southeast Brazil»
- ↑ «Portal da sociedade de dermatologia - Hanseníase»
- ↑ Diório, Suzana Madeira. Aspectos microbiológicos e moleculares do Mycobacterium leprae. [S.l.: s.n.] pp. Hanseníase – Avanços e Desafios
- ↑ «Níveis de Biossegurança»
- ↑ «Massive gene decay in the leprosy bacillus»
- ↑ «A New Model for Studying the Effects of Mycobacterium leprae on Schwann Cell and Neuron Interactions»
- ↑ Masaki, T. (2013). Reprogramming adult Schwann cells to stem celllike cells by leprosy bacilli promotes dissemination of infection. [S.l.: s.n.] pp. 51–67
- ↑ «Cellular microbiology: Mycobacterium leprae turns back the clock»